حلال ماده ای شیمیایی است که ماده شیمیایی دیگری را حل میکند و محلولی را به شکل مخلوط همگن تشکیل میدهد. بر اساس خصوصیات فیزیکی و شیمیایی انواع حلال شیمیایی وجود دارد. دسته حلال های آلی و معدنی بر اساس وجود کربن، دسته حلال های قطبی و غیر قطبی بر اساس ثابت دی الکتریک و دسته حلال های پروتیک و اپروتیک بر اساس پیوند هیدروژنی. در هنگام فروش مواد شیمیایی ممکن است یک ماده مانند آب در چندین دسته قرار بگیرد. آنها با توجه به خصوصیات فیزیکی و شیمیایی خود میتوانند موادی را به صورت مایع یا گاز داشته باشند و از این رو در فرآیندهای مختلفی مانند تولید دارو، رنگ، پوشش، چسب، شستشوی صنعتی و … استفاده میشوند.
حلالهای شیمیایی بر اساس ساختار، قطبیت و خواص فیزیکی به دستههای مختلفی تقسیم میشوند که در جدول زیر بهصورت خلاصه آمده است:
| معیار دسته بندی | انواع حلال | مثال |
| ساختار شیمیایی | آلی/معدنی | اتانول/آب |
| قطبیت | قطبی/غیر قطبی | متانول/هگزان |
| پیوند هیدروژنی | پروتیک/آپروتیک | آب/DMSO |
| منبع تولید | نفتی/زیستی | تولوئن/اتانول زیستی |
| ساختار مولکولی | آلیفاتیک/آروماتیک | هگزان/بنزن |
| فراریت | کم جوش/پرجوش | استون/DMSO |
| سمیت | کم خطر/ سمی | آب/بنزن |
حلال شیمیایی چیست؟
حلال شیمیایی (Solvent) موادی هستند که در فرآیندهای شیمیایی و صنعتی برای حل کردن، مخلوط کردن و استخراج مواد مورد نیاز استفاده میشوند. حلال های شیمیایی جزء موجود در محلول است که بیشترین مقدار را دارد و شکل فیزیک و شیمیایی ماده را به صورت جامد، مایع یا گاز تعیین میکند. به عبارت دیگر، حلال های شیمیایی بخشی است که معمولاً بیش از 50 درصد یک محلول را تشکیل میدهد، در حالی که املاح حل شونده بخشی است که در حلال مخلوط میشود. به طور معمول، بخش حل شونده کمتر از 50٪ محلول است. حلالها معمولاً مایع هستند و همچنین میتوانند گاز یا جامد باشند.
انتخاب حلال مناسب
انتخاب حلال مناسب به نوع موادی که باید حل شوند و شرایط مورد استفاده بستگی دارد. از ویژگیهای مهمی که در انتخاب انواع حلال باید در نظر گرفته شود میتوان به حلالیت، پایداری شیمیایی، قابلیت بازیافت، سمیت و سازگاری با محیط اشاره کرد. استفاده اصولی و رعایت نکات ایمنی در استفاده از انواع حلال شیمیایی بسیار مهم است. شامل استفاده در مکانهایی با تهویه مناسب، استفاده از تجهیزات حفاظت شخصی مناسب مانند دستکش و عینک ایمنی و دسترسی به اطلاعات ایمنی، برچسبها و فایلهای اطلاعاتی برای هر حلال است.
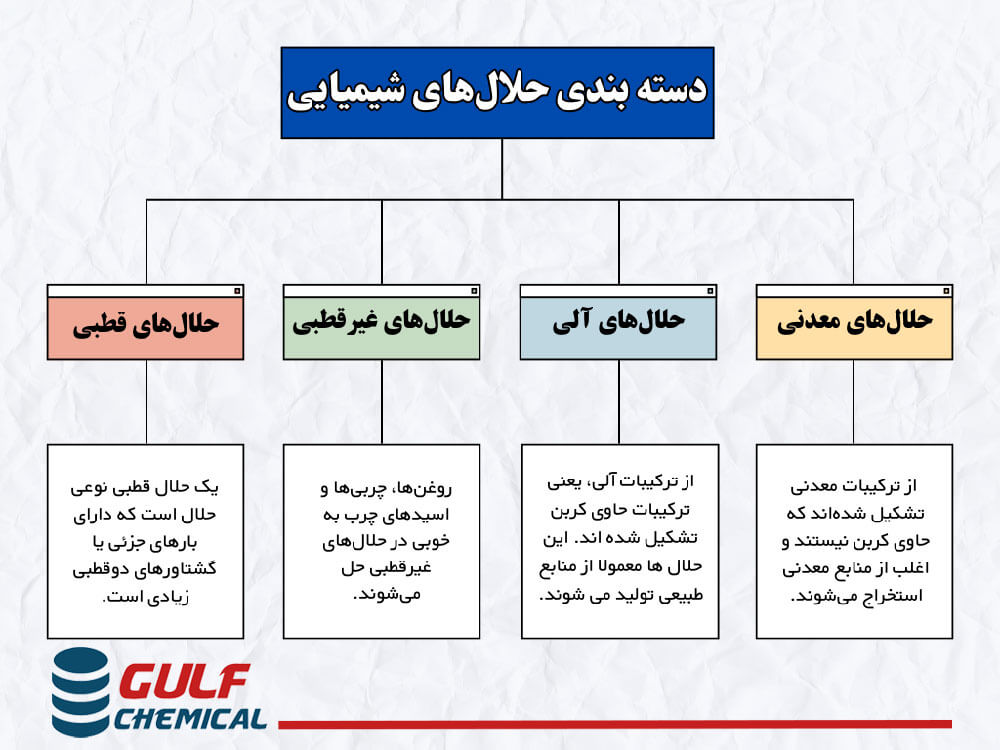
دسته بندی انواع حلال شیمیایی بر اساس ساختار
در ابتدا به دلیل وجود یا عدم وجود کربن در انواع حلال میتوان آنها را به دو دسته حلالهای آلی و حلالهای معدنی تقسیم کرد. در ادامه به توضیح هر یک میپردازیم:
1- حلال آلی چیست ؟
حلالهای آلی از ترکیبات آلی، یعنی ترکیباتی که حاوی کربن هستند، تشکیل شده اند. این حلالها معمولا از منابع طبیعی مانند نفت، گاز طبیعی، زغال سنگ و سایر منابع آلی تولید میشوند. انواع حلال الی عبارتند از الکلها، استرها، کتونها، اترها، بنزن، تولوئن و هیدروکربنهای معطر.
در دسته بندی حلال های شیمیایی حلالهای آلی خواص و کاربردهای مختلفی دارند. آنها را میتوان در صنایع مختلف مانند صنایع شیمیایی، فرآیندهای تولید، استخراج، تمیز کردن، رنگرزی و تمیز کردن مواد استفاده کرد. به عنوان مثال، الکلها به عنوان حلالهای رایج در صنعت رنگ و آزمایشگاهها و بنزن به عنوان حلال در تولید پلاستیک، رنگ و سایر مواد شیمیایی استفاده میشود.
لیست حلال های آلی
| انواع حلال الی | فرمول شیمیایی | کاربرد انواع حلال |
| استون (Acetone) | CH₃COCH₃ | تمیزکاری، لاکپاککن، واکنشهای آلی |
| اتانول (Ethanol) | C₂H₅OH | ضدعفونی، حلال دارویی و آرایشی، عصارهگیری |
| متانول (Methanol) | CH₃OH | سنتز آلی، ضدیخ، سوخت صنعتی، حلال قطبی |
| ایزوپروپانول (Isopropyl alcohol) | C₃H₈O | تمیزکننده تجهیزات الکترونیکی، ضدعفونیکننده |
| تولوئن (Toluene) | C₆H₅CH₃ | حلال رنگ، رزین، چسب، سوختهای افزودنی |
| هگزان | C₆H₁₄ | استخراج روغنهای گیاهی، کروماتوگرافی، شستوشو |
| دیاتیل اتر | C₄H₁₀O | حلال استخراج، واکنشهای آلی |
| کلروفرم | CHCl₃ | استخراج ، واکنشهای خاص در آلی |
| استات اتیل | CH₃COOC₂H₅ | صنایع رنگ، چسب، چاپ، داروسازی |
| آسیتونیتریل | CH₃CN | کروماتوگرافی HPLC، سنتز آلی، استخراج |
| زایلن | C₆H₄(CH₃)₂ | صنایع رنگ، پلاستیک، تینر، چسب |
2- حلالهای معدنی
در طبقه بندی حلال ها، حلالهای معدنی از ترکیبات غیرآلی (معدنی) تشکیل شدهاند که حاوی کربن نیستند و اغلب از منابع معدنی استخراج میشوند. این حلالها معمولاً شاملآب، اسیدها، بازها و مواد معدنی حلشده در آنها هستند. برخی از نمونههای رایج حلالهای معدنی شامل آب، اسید سولفوریک، اسید هیدروکلریک، آمونیاک و هیدروژن پراکسید هستند. انواع حلال معدنی در صنایع مختلف مورد استفاده قرار میگیرند. آنها میتوانند در استخراج معادن، فرآیندهای پالایش فلزات، صنایع پاککننده، تولید باتری، صنعت الکترونیک و صنایع داروسازی استفاده شوند. به عنوان مثال، اسید سولفوریک در صنعت پالایش نفت و تولید باتری و آب در صنایع غذایی، الکترونیک و تولید برق استفاده میشود.

دسته بندی حلال های شیمیایی براساس قطبیت
حلال قطبی و غیر قطبی چیست؟
همچنین، انواع حلال را میتوان از نظرثابت دیالکتریک به دو دسته تقسیم کرد: حلالهای قطبی و غیرقطبی. طور کلی، در انواع حلال شیمیایی ثابت دیالکتریک یک حلال، اندازهگیری تقریبی از قطبیت حلال را ارائه میدهد. یک حلال قطبی نوعی حلال است که دارای بارهای جزئی یا گشتاورهای دوقطبی زیادی است. پیوندهای بین اتمها دارای الکترونگاتیویتههای بسیار متفاوت اما قابل اندازهگیری هستند.
1- حلالهای قطبی
در تقسیم بندی حلال های شیمیایی یک حلال قطبی میتواندیونها و سایر ترکیبات قطبی راحل کند. در واقع، حلالهای قطبی مولکولهای دوقطبی قوی هستند که از طریق پیوند هیدروژنی با سایر مواد برهمکنش دارند. حلالهای قطبی همچنین اغلب پیوندهای کووالانسی حلشوندهها را میشکنند و این حلشوندهها را یونیزه میکنند. رایجترین حلالهای مورد استفاده در سیستمهای دارورسانی، انواع حلال قطبی از جمله آب و الکل هستند. میتوان به سایر حلالهای قطبی مانند الکلها، آلدئیدها و کتونهای قندی و سایر ترکیبات دارای گروههای OH- نیز اشاره کرد.
یک مورد خاص، جیوه است که محلولهای آن به عنوان ملغمه شناخته میشوند. همچنین محلولهای فلزی دیگری نیز وجود دارند که در دمای اتاق مایع هستند.
لیست حلالهای قطبی
| لیست حلال های قطبی | فرمول شیمیایی | قطبیت | کاربرد انواع حلال قطبی |
| آب | H₂O | قطبیت بسیار بالا | ترکیبات یونی و قطبی، استفاده در صنایع غذایی، دارویی، و شیمیایی |
| اتانول | C₂H₅OH | قطبیت بالا | تولید عطرها، صنایع داروسازی، صنایع غذایی |
| استون | CH₃COCH₃ | قطبیت متوسط | لاک پاککنها، تولید پلاستیک، تمیزکاری و صنایع رنگ |
| متانول | CH₃OH | قطبیت بالا | تولید سوختهای زیستی، ضدیخ، و حلال در سنتز مواد شیمیایی |
| استیک اسید | CH₃COOH | قطبیت بالا | تولید پلیمرها، نگهدارنده مواد غذایی |
| دیمتیل فرمآمید (DMF) | HCON(CH₃)₂ | قطبیت بالا | سنتز مواد شیمیایی و دارویی، تولید پلاستیک و فیلمهای پلیمری |
| دیمتیل سولفوکساید (DMSO) | C₂H₆OS | قطبیت بالا | حلال برای ترکیبات آلی و دارویی، استفاده در آزمایشگاههای شیمیایی |
| تتراهیدروفوران (THF) | C₄H₈O | قطبیت متوسط | حلال در سنتز پلیمرها و واکنشهای آلی |
| نیترومتان | CH₃NO₂ | قطبیت بالا | حلال در واکنشهای شیمیایی، سوختهای ویژه، و سنتز ترکیبات دارویی |
| فرمالدئید | HCHO | قطبیت بالا | استفاده در سنتز رزینها، مواد نگهدارنده و ضدعفونیکننده |
| ایزوپروپانول | C₃H₈O | قطبیت متوسط | حلال در ضدعفونیکنندهها، داروسازی، و تمیزکاری صنعتی |
| پروپیلن گلیکول | C₃H₈O₂ | قطبیت متوسط | استفاده در صنایع آرایشی و بهداشتی، مواد خوراکی، و حلال دارویی |
| اتیلن گلیکول | C₂H₆O₂ | قطبیت بالا | حلال در ضدیخها، خنککنندهها و تولید رزینهای پلیاستر |
| پروپانول (1-پروپانول) | C₃H₇OH | قطبیت متوسط | حلال در محصولات بهداشتی، دارویی و صنایع شیمیایی |
2- حلالهای غیرقطبی
در دسته بندی حلال های شیمیایی حلال غیرقطبیخواص دوقطبی کمی دارند یا اصلاً ندارند. اگرچه آنها نمیتوانند به طور مستقل دوقطبی تشکیل دهند، اما میتوانند از برهمکنشهای دوقطبی-دوقطبی برای حل کردن حلشوندههای مناسب استفاده کنند. در لیست حلال های شیمیایی حلالهای غیرقطبی دارای ثابت دیالکتریک بین ۱ و ۲۰ هستند و شامل روغنهای ثابت، تتراکلرید کربن و کلروفرم میشوند. حلشوندههای یونی و قطبی حلالیت کمی در حلالهای غیرقطبی دارند یا اصلاً حل نمیشوند. با این حال، روغنها، چربیها و اسیدهای چرب به خوبی در حلالهای غیرقطبی حل میشوند.
لیست حلالهای غیر قطبی
| لیست حلال های غیر قطبی | فرمول شیمیایی | کاربرد انواع حلال غیر قطبی |
| هگزان | C₆H₁₄ | استخراج روغنهای گیاهی، تمیزکاری صنعتی و چربیزدایی |
| پنتان | C₅H₁₂ | یک حلال غیر قطبی در صنایع پلاستیکسازی، عایقسازی و تولید فومهای پلییورتان |
| تولوئن | C₆H₅CH₃ | تولید رنگها، چسبها و به عنوان ماده اولیه در صنایع شیمیایی |
| بنزن | C₆H₆ | صنایع شیمیایی و تولید مواد آلی اما به دلیل سمی بودن کاربرد محدودی دارد |
| کربن تتراکلرید ناقطبی | CCl₄ | حلال غیر قطبی در تمیزکاری خشک، خنککننده در سیستمهای قدیمی و استخراج ترکیبات شیمیایی |
| کلروفرم | CHCl₃ | استخراج ترکیبات دارویی و در آزمایشگاههای شیمیایی |
| اتر دیمتیل | C₂H₆O | سنتز آلی و به عنوان گاز در افشانهها |
| سیکلوهگزان | C₆H₁₂ | تولید نایلون و به عنوان ماده واسطه در سنتز شیمیایی |
| هپتان | C₇H₁₆ | آزمایشهای کالیبراسیون و تمیزکاری تجهیزات حساس |
| دیاتیل اتر | C₄H₁₀O | سنتز آلی، استخراج مواد و به عنوان بیحسکننده در گذشته |
دسته بندی حلال های شیمیایی بر اساس پیوند هیدروژنی
1- حلال پروتیک
انواع حلال پروتیک نوعی حلال الی است که میتواند یک یا چند گروه پروتون (H+) قابل انتقال داشته باشد. این حلالها معمولاً از ترکیباتی با خاصیت اسیدی تشکیل شدهاند و قادر به ایجاد پیوندهای هیدروژنی هستند. گروه پروتون میتواند به صورت یونیزه (مانند یون هیدروژن H+) یا غیر یونیزه (مانند گروه هیدروکسیل OH) در حلال پروتیک وجود داشته باشد. برخی از نمونههای شناخته شده حلالهای پروتیک عبارتند از آب (H2O)، الکلها مانند متانول (CH3OH) و اتانول (C2H5OH)، اسید استیک (CH3COOH) و آمونیاک (NH3).
در طبقه بندی حلال های شیمیایی حلالهای پروتیک به دلیل گروه پروتون قابل انتقال خود، قادر به تحویل پروتون به سایر ترکیبات در فرآیندهای شیمیایی هستند. همچنین، این حلالها توانایی ایجاد پیوندهای هیدروژنی با سایر مواد را دارند که میتواند تأثیر زیادی بر رفتار و خواص مواد در محلول داشته باشد. استفاده از حلالهای پروتیک در بسیاری از فرآیندهای شیمیایی و بیولوژیکی بسیار رایج است.
آب به عنوان یک حلال پروتیک بسیار مهم در اکثر فرآیندهای بیولوژیکی و شیمیایی استفاده میشود و خواص منحصر به فردی دارد که آن را از سایر حلالها متمایز میکند. در حالی که یک حلال پروتیک قادر به تشکیل پیوندهای هیدروژنی است، یک حلال آپروتیک به عنوان دهنده پیوند هیدروژنی عمل نمیکند. انواع حلال آپروتیک معمولاً قطبیت کمتری دارند و نمیتوانند پروتون را به سایر ترکیبات منتقل کنند.
2- حلال آپروتیک
در دسته بندی حلال های شیمیایی حلال آپروتیک نوعی حلال شیمیایی است که توانایی تشکیل پیوندهای هیدروژنی را به طور کامل یا جزئی ندارد. در این حلالها، معمولاً عدم وجود گروههای پروتون قابل انتقال مانند گروه هیدروکسیل (OH) باعث میشود که آنها نتوانند به عنوان دهنده پیوند هیدروژنی عمل کنند. انواع حلال آپروتیک معمولاً قطبیت کمتری نسبت به حلالهای پروتیک دارند. این بدان معناست که یونهای پروتون قابل انتقال (H+) وجود ندارند.
نمونههای حلالهای آپروتیک در لیست حلال های شیمیایی
- اترها مانند دی اتیل اتر (C2H5OC2H5)
- متیلن کلرید (CH2Cl2)
- کتونها مانند استون (CH3COCH3)
- نیتریلها مانند استیرن نیتریل (C6H5CN)

کاربرد حلال آپروتیک
در دسته بندی حلال های شیمیایی حلالهای آپروتیک به دلیل عدم توانایی در تشکیل پیوندهای هیدروژنی، در برخی از فرآیندهای شیمیایی بسیار مفید هستند. آنها میتوانند به عنوان حلالهای مناسب برای واکنشهایی که نیاز به جداسازی یونها دارند، استفاده شوند. همچنین، انواع حلال آپروتیک ممکن است انتخاب خوبی در فرآیندهایی باشند که به رطوبت و وجود آب حساس هستند.
مزیت دیگر حلالهای آپروتیک این است که آنها به طور کلی در دماهای بالا پایدارتر هستند و تبخیر کمتری دارند. این میتواند در فرآیندهایی که نیاز به دماهای بالا دارند، بسیار مهم باشد. به طور کلی، استفاده از حلالهای آپروتیک و پروتیک بسته به نیازهای واکنش و خواص مواد در سیستم شیمیایی متفاوت است و انتخاب صحیح حلال برای هر فرآیند و واکنش خاص نیاز به توجه ویژه دارد.
حلال های شیمیایی زیستی در صنعت بیوتکنولوژی
در طبقه بندی حلال ها ترکیباتی هستند که در طبیعت وجود ندارند. تعداد محدودی حلال شیمیایی با منشأ زیستی وجود دارد، مانند اتانول، بوتانول و استون. ترپنها نیز حلالهای طبیعی تولید شده توسط گیاهان هستند. این حلالها معمولاً برای سلولهای میکروبی سمی هستند. در صنایع شیمیایی، از انواع حلال برای تماس با میکروارگانیسمها استفاده میشود. اما در صنایع بیوتکنولوژی، به دلیل ترجیح میکروارگانیسمها به آب و مشکلاتی که حلالهای شیمیایی برای سلولها ایجاد میکنند، از سیستمهای مبتنی بر آب استفاده میشود. حلالهای شیمیایی اغلب برای استخراج محصولات از فاز آبی استفاده میشوند، اما در این مرحله آسیب به سلولها مهم نیست. هم در صنایع شیمیایی و هم در صنایع بیوتکنولوژی، حلال الی نسبت به آب مزایایی دارند.
دسته بندی حلالهای نفت و گاز بر اساس وزن مولکولی هیدروکربن
نفت و گاز طبیعی منابع فراوان و مقرونبهصرفه هیدروکربنها هستند. اصطلاح «نفت خام» گاهی برای اشاره به نفت مایع با نقطه جوش پایین و محصولات گاز طبیعی مایع با محدوده جوش ۱۵.۶ درجه سانتیگراد تا ۲۲۱ درجه سانتیگراد استفاده میشود. این ترکیبات به ساختارهای آلیفاتیک و آروماتیک تقسیم میشوند. هیدروکربنهای آلیفاتیک شامل پارافینها، اولفینها، آلکینها و سیکلوپارافینها هستند. پارافینها میتوانند خطی (مانند نرمال بوتان، نرمال پنتان و نرمال هگزان) یا شاخهدار (مانند ایزوبوتان، ایزوپنتان و ایزوهگزان) باشند. اولفینها نمونهای از آنها هستند و اتیلن مشهورترین نمونه آن است. سیکلوپارافینها شامل سیکلوپنتان و سیکلوهگزان هستند.

پس از پالایش، نفت خام به گازهای هیدروکربنی، تقطیرات سبک، تقطیرات میانی، تقطیرات سنگین و مواد باقیمانده تقسیم میشود. این تقسیمبندی بر اساس وزن مولکولی هیدروکربنها است و در دسته بندی حلال های شیمیایی شامل موادی مانند متان، اتان، پروپان، بوتان، نفتا، روغنهای تصفیهشده، نفت گاز، روغن جاذب، روغنهای صنعتی، موم پارافین، روغنهای روانکننده، آسفالت، کک، لجن پالایشگاه و مواد دیگر است.
کاربرد حلال های شیمیایی
حلالها کاربردهای گستردهای از کارهای معمولی خانگی گرفته تا کارهای صنعتی دارند. آنها به طور وسیعی برای حل کردن روغن، رنگها، مخلوط کردن رنگدانهها، چسبها و رزینها استفاده میشوند و همه اینها کاربردهای خاص خود را دارند. آنها در تمیز کردن قطعات خودرو، الکترونیک، رنگآمیزی، مخلوط کردن مواد شیمیایی و غیره استفاده میشوند. آنها طیف وسیعی از کاربردها در صنایع شیمیایی، دارویی، نفت و گاز، از جمله سنتز و خالصسازی شیمیایی دارند.
موارد زیر در طبقه بندی حلال های شیمیایی در فرآیند تولید استفاده میکنند:
- داروسازی
- پوششها و رنگها
- جوهر برای چاپ
- مراقبت شخصی و لوازم آرایشی
- غذا و نوشیدنی
- چربیزدایی و تمیز کردن
پرکاربردترین حلال ها در صنعت
| انواع حلال شیمیایی | نکات مهم | کاربردهای رایج | دسته و زیر دسته ها |
| آب (H₂O) متانول (CH₃OH) اتانول (C₂H₅OH) اسید استیک (CH₃COOH) | آب یکی از رایج ترین حلالهای قطبی است و از الکل در صنایع غذایی و داروسازی استفاده میشود. | حل کردن نمکها، قندها، اسیدها و بازها، واکنشهای شیمیایی قطبی | حلال آپروتیک که دارای هیدروژن متصل به اکسیژن و نیتروژن است. جزء حلالهای قطبی |
| استون (CH₃COCH₃) دیمتیل سولفوکسید (DMSO) دیمتیل فرمآمید (DMF) | استون به عنوان پاککننده و در صنایع شیمیایی استفاده میشود. دی متیل سولفوکسید و دی متیل فرمآمید حلالهای قوی برای واکنشهای شیمیایی خاص هستند. | حل کردن ترکیبات قطبی، واکنشهای شیمیایی که نیاز به محیط آپروتونی دارند | حلالهای آپروتونی بدون هیدروژنِ متصل به اکسیژن یا نیتروژن، اما دارای قطبیت جزء حلالهای قطبی |
| هگزان (C₆H₁₄) پنتان (C₅H₁₂) سیکلوهگزان (C₆H₁₂) | در صنایع نفت و پتروشیمی و همچنین استخراج روغن از دانهها کاربرد دارند. | حل کردن روغنها، چربیها، مومها و ترکیبات ناقطبی | هیدروکربنهای آلیفاتیک جزء حلال غیر قطبی |
| بنزن (C₆H₆) تولوئن (C₆H₅CH₃) زایلن (C₆H₄(CH₃)₂) | تولوئن در رنگها و چسبها استفاده میشود. بنزن به دلیل سمی بودن کاربرد محدودی دارد. | حل کردن لاستیک، رزین، رنگها و برخی از ترکیبات آلی | هیدروکربنهای آروماتیک جزء حلال غیر قطبی |
| کلروفرم (CHCl₃) دیکلرومتان (CH₂Cl₂) تتراکلرید کربن (CCl₄) | به دلیل سمیت، استفاده از آنها محدود شده است. دیکلرومتان به عنوان حلال در برخی از فرآیندهای صنعتی استفاده میشود. | حل کردن چربیها، روغنها و برخی از پلیمرها | هالوژندارها |
| اتیل استات (CH₃COOC₂H₅) بوتیل استات (CH₃COO(CH₂)₃CH₃) | در صنایع رنگ، چسب و عطر استفاده میشوند. | حل کردن نیتروسلولز، رزینها و برخی از پلیمرها | استرها |
| دیاتیل اتر (CH₃CH₂OCH₂CH₃) تتراهیدروفوران (THF) | THF حلال قطبی آپروتونی است که در واکنشهای شیمیایی کاربرد دارد. | حلالهای خوب برای واکنشهای گرینیارد و سایر واکنشهای شیمیایی | اترها |
نتیجه گیری
حلال های شیمیایی ترکیباتی هستند که برای حل و انتقال مواد در فرآیندهای شیمیایی و صنعتی استفاده میشوند. حلالهای آبی، حلالهای آلی، حلالهای هیدروکربنی و حلالهای بیولوژیکی از انواع حلال های شیمیایی هستند. این حلالها دارای مزایا و کاربردهای مختلفی مانند استخراج، سنتز شیمیایی، تمیز کردن و رنگ زدایی هستند. انتخاب حلال مناسب به خواص ماده ای که باید حل شود و نیازهای فرآیند بستگی دارد. هنگام استفاده از حلال های شیمیایی به جنبههای بهداشتی، ایمنی و زیست محیطی توجه کنید و با دقت عمل کنید.
سوالات متداول در مورد حلال های شیمیایی
فراوان ترین و مهمترین حلال در طبیعت چیست ؟
آب به دلیل فراوانی در طبیعت ، تشکیل پیوند هیدروژنی ، قطبیت بالا و حل کردن بسیاری از مواد شیمیایی معروفترین حلال است و در صنعت ، آزمایشگاه ، زیست شناسی و محیط زیست کاربرد زیادی دارد. از آنجایی که همه مواد شیمیایی در آب حل نمی شوند، در بسیاری از صنایع از اتانول ، استون و دی متیل سولفوکساید به عنوان حلال استفاده می شود.
استون قطبی است یا ناقطبی ؟
قطبی
مهمترین انواع حلال ها در زندگی روزمره کدامند؟
آب -متانول – اتانول -اسید استیک
چند نمونه از رایج ترین حلال های شیمیایی
هگزان (C₆H₁₄)
پنتان (C₅H₁₂)
سیکلوهگزان (C₆H₁₂)
بنزن (C₆H₆)
تولوئن (C₆H₅CH₃)
زایلن (C₆H₄(CH₃)₂)
حلال آلی چیست؟
نوعی ترکیب آلی فرار است که به عنوان حلال شامل ترکیبات آروماتیک، الکلها، کتونها، آمینها، هیدروکربنهای نیتراته و هالوژنه هستند.حلالهای آلی برای حل کردن مواد، پراکنده کردن پوششها، واسطه برای واکنشهای شیمیایی، عوامل تمیزکننده به کار می رود.
کربن تتراکلراید قطبی یا ناقطبی ؟
کربن تتراکلراید جز حلال های ناقطبی است. با وجود پیوند قطبی بین کربن و کلر ، تقارن مولکولی باعث صفر شدن گشتاور قطبی می شود.
دی متیل اتر قطبی یا ناقطبی؟
دی متیل اتر به دلیل داشتن اتم اکسیژن قطبی است. اما قطبیت آن از الکل ها کمتر است.
حلال کربن چیست؟
حلال کربن از هیدروژن و کربن تشکیل شده است که برای شستن آلاینده های روغنی، رسوبات چربی و سایر ترکیبات آلی به کار می رود. حلال کربن برای پاک سازی سطوح و تجهیزات صنعتی کاربرد دارد.
استیک اسید قطبی است یا ناقطبی؟
استیک اسید به دلیل داشتن گروه کربوکسیل قطبی و ثابت دی الکتریک بالا، قطبی است. همچنین انحلال پذیری کمی در حلال های غیر قطبی دارد که نشان دهنده ماهیت قطبی آن است.



عالی بود.
بهترین و کاملترین مقاله عالی بود♥️
از بین حلال های شیمیایی و لیست حلال های آلی ایزوپروپیل الکل برای تمیز کردن رنگ اکریلیک خشک شده بهترین گزینه است